Để giải các dạng bài xích tập Hóa về thể tích, khối lượng, số mol… các em buộc phải ghi nhớ những công thức tính thể tích hóa học cùng mối liên hệ giữa các đại lượng khớp ứng của công thức. Trong nội dung bài viết này, Marathon Education sẽ share đến các em các công thức tính thể tích hóa học thường gặp gỡ trong lịch trình Hóa phổ thông. Các em hãy coi kỹ, học thuộc và vận dụng vào nhằm “xử đẹp” các bài tập được giao hoặc gặp gỡ phải vào kỳ thi.
Bạn đang xem: Công thức tính thể tích hóa học

Tính thể tích bằng số mol
Trong đk chuẩn, thể tích hóa học khí bằng số mol nhân với 22,4, ta tất cả công thức cụ thể như sau:
V = n.22,4
Trong đó:
V là thể tích hóa học khí ở điều kiện chuẩn (l)n là số mol của chất khí sinh sống điều kiện chuẩn chỉnh (mol)Tính thể tích bằng khối lượng
Thể tích dung dịch hoặc chất được khẳng định bằng mến số giữa khối lượng dung dịch hoặc hóa học với khối lượng riêng của dung dịch hoặc hóa học đó, ta bao gồm công thức nắm thể:
Trong đó:V là thể tích hỗn hợp hoặc chất (m3)m là khối lượng dung dịch hoặc hóa học (kg)D là trọng lượng riêng của hỗn hợp hoặc hóa học (kg/m3)
Tính thể tích bởi nồng độ mol
Thể tích dung dịch được xác định bằng thương số thân số mol hóa học tan phân tách cho nồng độ mol của hỗn hợp đó, ta bao gồm công thức ví dụ là:
Trong đó:V là thể tích dung dịch (l)n là số mol chất tan (mol)CM là mật độ mol hỗn hợp (mol/l)
Tính thể tích ko khí
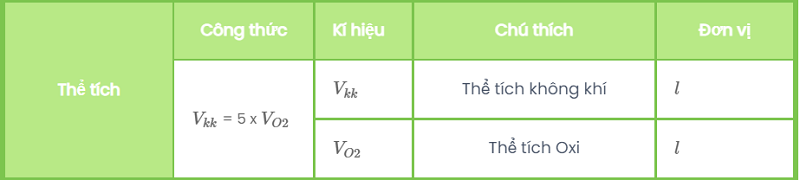
Thể tích không khí cấp 5 lần thể tích oxi, ta có công thức ví dụ như sau:
Vkk = 5.VO2
Trong đó:
Vkk là thể tích của bầu không khí (l)VO2 là thể tích của oxi (l)
Công thức tính khối lượng hóa học

Tính trọng lượng chất tan bằng số mol
Khối lượng chất tan ngay số mol nhân với cân nặng mol chất. Ta bao gồm công thức như sau:
m = n.M
Trong đó:
M là cân nặng chất rã (gam).n là số mol chất (mol).M là trọng lượng mol hóa học (gam).Tính khối lượng chất rã bằng trọng lượng dung dịch
Khối lượng chất tan được khẳng định bằng hiệu số cân nặng dung dịch trừ trọng lượng dung môi. Ta bao gồm công thức sau:
mct = mdd – mdm
Trong đó:
mct là khối lượng chất tung (g).mdd là cân nặng dung dịch (g).mdm là khối lượng dung môi (g).Tính cân nặng dung dịch bằng trọng lượng chất tan
Khối lượng dung dịch bằng cân nặng chất tung nhân nồng độ phần trăm. Ta gồm công thức sau đây:
hoặc mdd = mct + mdm
Trong đó:
mdd là cân nặng dung dịch (g)mct là khối lượng chất tung (g)C% là nồng độ phần trăm (%)mdm là trọng lượng dung môi (g)Tính trọng lượng dung dịch bằng thể tích
Công thức tính trọng lượng dung dịch được xác định bằng thể tích nhân với trọng lượng riêng. Ta có:
mdd = V. D
Trong đó:
mdd là khối lượng dung dịch (g)V là thể tích dung dịch (ml)D là cân nặng riêng dung dịch (g/ml)Bài tập vận dung bí quyết tính thể tích và khối lượng hóa học
Bài tập 1: Tính thể tích 8 g khí oxi sinh sống đktc.
Lời giải:
Số mol phân tử O2: n
O2 = m
O2/MO2 = 8/32 = 0,25 mol
Thể tích 8g khí oxi ngơi nghỉ đktc: VO2 = n
O2.22,4 = 0,25.22,4 = 5,6 l
Bài tập 2: Tính trọng lượng của 8,96 lít khí CO2 ở đktc.
Lời giải:
Số mol phân tử CO2: n
CO2 = VCO2/22,4 = 8,96/22,4 = 0,4 mol
Khối lượng của 8,96 lít khí CO2 ở đktc: VCO2 = n
CO2.n
CO2 = 0,4.44 = 17,6 g
Bài tập 3: Một tất cả hổn hợp khí A tất cả 0,25 mol khí SO2 và 0,15 mol khí CO2
cam kết Hiệu hóa học Là Gì? những Ký Hiệu hóa học Lớp 8 Đầy Đủ, chi Tiết
a. Tính thể tích của tất cả hổn hợp khí A (đktc).
b. Tính cân nặng của tất cả hổn hợp khí A.
Lời giải:
a. Thể tích của hỗn hợp khí A (đktc):
VA = n
A.22,4 = (0,25 + 0,15).22,4 = 8,96 l
b. Cân nặng của hỗn hợp khí A:
m
A = m
SO2 + m
CO2 = n
SO2.MSO2 + n
CO2.MCO2 = 0,25.64 + 0,15.44 = 22,6 g
Tham khảo ngay các khoá học online của Marathon Education
Gia sư Online
Học Online Toán 12
Học Online Hóa 10
Học Online Toán 11
Học Online Toán 6
Học Online Toán 10
Học Online Toán 7
Học Online Lý 10
Học Online Lý 9
Học Online Toán 8
Học Online Toán 9
Học tiếng Anh 6
Học giờ Anh 7
Mong rằng phần lớn nội dung về công thức tính thể tích hóa học và trọng lượng ở trên sẽ giúp các em hoàn toàn có thể vận dụng vào giải bài tập hiệu quả. Ngoài ra, những em cũng có thể học trực tuyến online thêm nhiều kỹ năng và kiến thức Toán – Lý – Hóa hữu ích khác trên website Marathon Education. Chúc những em luôn học tập xuất sắc và được điểm cao trong các bài bình chọn cùng bài bác thi!
CÓ THỂ BẠN quan lại TÂM

Top 33+ công thức Hóa học tập Lớp 8-12 ➤ 4 Mẹo Ghi Nhớ hết sức Nhanh

Bảng Tuần Hoàn những Nguyên Tố Hóa Học: cách Học cùng Mẹo Ghi Nhớ

Học Hóa Lớp 10 Trực đường Với giáo viên Top 1%
Lý Thuyết Ankadien Hóa 11: Định Nghĩa, tính chất Và Điều Chế Ankadien
Lý Thuyết Anken: Khái Niệm, Danh Pháp và Phản Ứng Đặc Trưng Của Anken
Lý Thuyết Ankan: Định Nghĩa, đặc điểm Vật Lý, tính chất Hóa học tập Ankan
Marathon – căn cơ lớp học trực tuyến đường hàng đầu, cung cấp giải pháp giáo dục toàn diện ngoài trường học mang đến tất cả học viên trên toàn nước với quality tốt nhất!Tìm gọi thêm về Marathon tại:
Thông tin yêu cầu thiết
Địa chỉ 1: Tầng 9, Tòa công ty Lim Tower 3, 29A Nguyễn Đình Chiểu, Phường Đa Kao, Quận 1, TP. Hồ Chí Minh.
Địa chỉ 2: tầng trệt dưới – 3 ,Tòa công ty Yoko Building, 677/6 Điện Biên Phủ, Phường 25, Quận Bình Thạnh, TP. Hồ Chí Minh
Các phân mục chính
Đội Ngũ Giáo Viên
Các lớp học
Lớp Đánh giá bán Năng Lực
Lớp thầy giáo Marathon
Câu chuyện về Marathon
Affiliate
Thông tin liên hệ
Hotline: (028) 7300 3033
Tất cả ngôn từ thuộc bản quyền của Marathon
Education
Terms và Conditions
Privacy Policy
Công thức tính thể tích hoá học là 1 trong trong số những bí quyết mà những em đang thường bắt gặp trong môn hoá. Để nắm vững được kỹ năng và kiến thức này, hãy thuộc Bamboo School mày mò nhé.
Thể tích là gì?
Thể tích của một vật là lượng không khí mà một thứ đó chiếm.
Chẳng hạn như dòng cốc gồm dung tích là 450ml nhưng mà thể tích nước vào cốc chỉ chiếm khoảng gần 400ml như hình mặt dưới.

Kí hiệu của thể tích
Đơn vị đo thể tích hóa học lỏng thường được sử dụng là mét khối m^3 với lít (l)
Các phương pháp tính thể tích chất hóa học cơ bản
Tính thể tích biết trọng lượng riêng
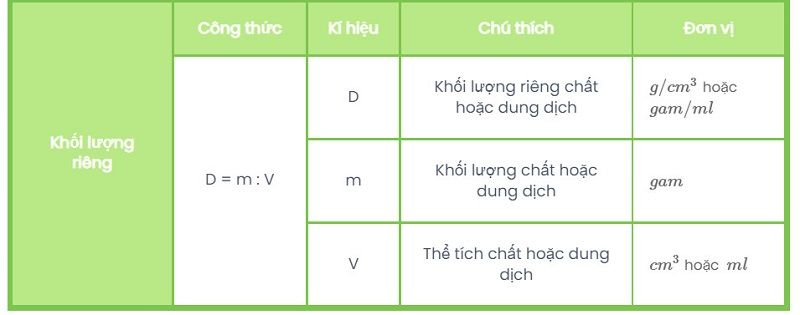
Tính thể tích khi biết số mol
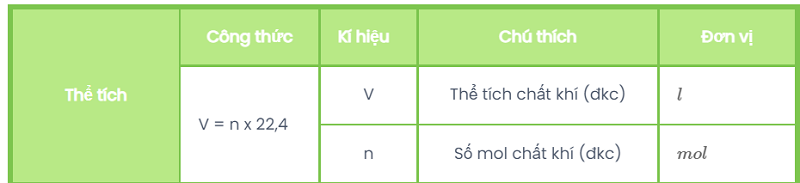
Tính thể tích khi biết khối lượng
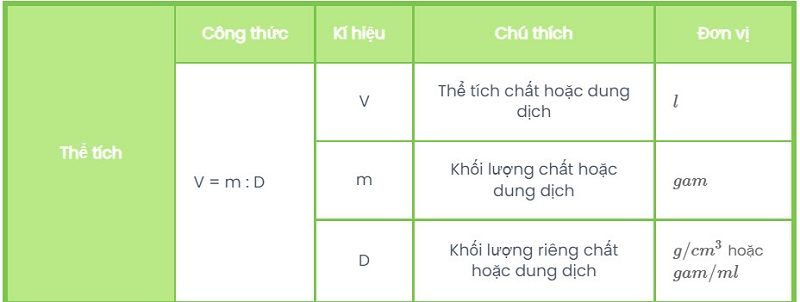
Tính thể tích lúc biết nồng độ Mol của dung dịch
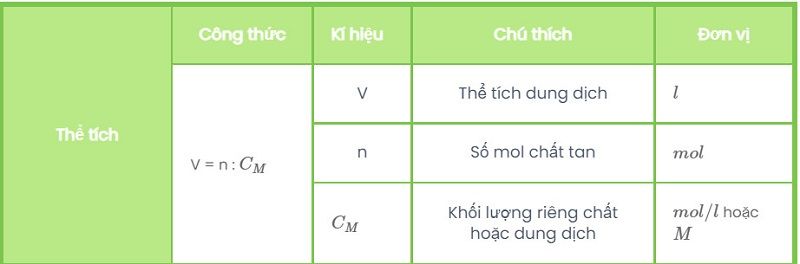
Tính thể tích khi biết thể tích Oxi
Các bài bác tập tính thể tích hóa học cơ bạn dạng có đáp án
Ví dụ 1: Hãy tính thể tích của 6,8g khí oxi nghỉ ngơi đktc?
Bài giải:
Khối lượng mol của O2 là: MO2 = 16.2 = 32 g/mol
Số mol phân tử O2 là: n
O2 =
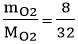
Thể tích của 8g khí oxi làm việc đktc là:
VO2 = n
O2 . 22,4 = 0,25.22,4 = 5,6 lít.
Ví dụ 2: Tính trọng lượng của 8,96 lít khí CO2 ở đktc?
Bài giải:
Số mol phân tử CO2 là: n
CO2 =
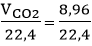
Khối lượng mol của CO2 là: MCO2 = 12 +16.2 = 44 g/mol
Khối lượng của 8,96 lít khí CO2 ở đktc là:
m
CO2 = n
CO2.MCO2 = 0,4.44 = 17,6 gam.
Ví dụ 3: Một hỗn hợp khí X bao gồm 0,25 mol khí SO2 và 0,15 mol khí CO2
a) Tính thể tích của tất cả hổn hợp khí X (đktc).
b) Tính trọng lượng của tất cả hổn hợp khí X.
Bài giải:
a) Thể tích của hỗn hợp khí X (đktc) là:
VX = n
X.22,4 = (0,25 + 0,15).22,4 = 8,96 lít
b) MCO2 = 32 + 2.16 = 64 g/mol
Khối lượng của 0,25 mol khí SO2 là: m
CO2 = n
CO2.MCO2 = 0,25.64 = 16g.
MCO2 = 12+2.16 = 44 g/mol
Khối lượng của 0,15 mol khí CO2 là: m
CO2 = n
CO2.MCO2 = 0,15.44 = 6,6g.
Khối lượng của các thành phần hỗn hợp khí X là: m
X = m
CO2 + m
CO2 = 16 +6,6 = 22,6g.
Xem thêm: Hệ Thống Các Công Thức Toán 12 Hình Học 12 Từ Căn Bản Tới Nâng Cao
Ví dụ 4: Phải lấy từng nào lít khí CO2 ở đktc để sở hữu 3.1023 phân tử CO2?
Bài giải:
3.1023 phân tử CO2 ứng với số mol là:
n
CO2 =
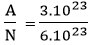
Thể tích khí CO2 ở đktc để có 3.1023 phân tử CO2 là:
VCO2 = n
CO2. 22,4 = 0,5.22,4 = 11,2 lít
Ví dụ 5: 0,75 mol phân tử H2S chỉ chiếm thể tích từng nào lít (đo sinh sống đktc)?
Bài giải:
Thể tích của 0,75 mol phân tử H2S đo sinh sống đktc là:
VH2S = n
H2S. 22,4 = 0,75.22,4 = 16,8 lít
Hy vọng phương pháp tính thể tích hoá học nhưng mà Bamboo School đã phân chia sẽ hoàn toàn có thể giúp các em phần nào nắm rõ được kiến thức của mình.