mythuatcongnghiepachau.edu.vn sẽ chia sẻ chuyên sâu kiến thức của Công thức hóa học của sắt 3 oxit là hi vọng nó sẽ hữu ích dành riêng cho quý các bạn đọc
Sắt(III) oxit Tên không giống Ferric oxit, Hematit, sắt oxit đỏ, synthetic maghemit, colcothar, sắt sesquioxit, ferrum(III) oxit ferrum sesquioxit thừa nhận dạng Số CAS 1309-37-1 Pub
Chem 518696 Số RTECS NO7400000 Ảnh Jmol-3D ảnh SMILES In
Ch
I Chem
Spider 21106565 ở trong tính công thức phân tử Fe2O3 cân nặng mol 159,6922 g/mol hình thức chất rắn màu đỏ nâu Mùi ko mùi trọng lượng riêng 5,242 g/cm³, rắn Điểm rét chảy 1.566 °C (1.839 K; 2.851 °F) (phân hủy) Điểm sôi Độ hòa tan trong nước ko tan cấu trúc Cấu trúc tinh thể cha nghiêng Nhiệt hóa học Entanpi xuất hiện Δf
Ho298 -825,50 k
J/mol Các nguy nan Phân loại của EU không phân nhiều loại Điểm bắt lửa không cháy các hợp chất tương quan Anion khác Sắt(III) florua Cation không giống Mangan(III) oxit Coban(III) oxit thích hợp chất tương quan
Công thức hóa học của fe III oxit.
Bạn đang xem: Công thức hóa học của sắt 3 oxit là
Sắt III oxit gồm 2 nguyên tố fe kết hơp với 3 yếu tố O.
Hợp hóa học sắt (III) oxit là đúng theo chất trong các số đó sắt bao gồm mức oxi hóa +3.
Sắt 3 Oxit là một trong oxide của sắt.
Công thức hóa học: Fe2O3
Phân tử khối: 160 g/mol.
Trong vật liệu gốm
Các hợp chất sắt là các chất chế tạo màu phổ biến nhất trong ngành gốm. Sắt hoàn toàn có thể biểu hiện khác biệt tùy thuộc môi trường xung quanh lò, nhiệt độ nung, thời hạn nung và tùy thuộc vào thành phần hoá học của men. Vày đó có thể nói rằng nó là trong số những nguyên liệu lý thú nhất.
Trong môi trường nung khử, Fe2O3 thuận tiện bị khử (do cacbon hay những hợp hóa học lưu huỳnh trong nguyên liệu, trong môi trường lò) thành Fe
O và trở thành chất chảy. Nếu như muốn giữ được sắt(III) oxit, từ bỏ 700-900 ℃, môi trường xung quanh nung yêu cầu là oxy hóa. Trong môi trường xung quanh nung oxy hóa, nó vẫn luôn là Fe2O3 và mang đến màu men tự hổ phách (amber) cho vàng trường hợp hàm lượng buổi tối đa trong men là 4% (rõ rệt hơn nếu men gồm chì oxit và can xi oxit), mang lại men màu da rám nắng nóng (tan) trường hợp hàm lượng khoảng chừng 6% và đến màu nâu nếu hàm lượng Fe2O3 cao hơn.
Màu đỏ của sắt(III) oxit gồm thể biến hóa trên một khoảng rộng trong khoảng nhiệt độ nung thấp bên dưới 1050 ℃. Trường hợp nung rẻ thì bao gồm màu cam sáng. ánh sáng tăng color sẽ đưa sang đỏ sáng sủa rồi đỏ sậm và sau cuối là nâu. Chuyển đổi từ đỏ sang trọng nâu xảy ra bất ngờ trên một khoảng chừng nhiệt độ hẹp, buộc phải lưu ý.
Hầu hết những loại men sẽ có độ hoà rã sắt(III) oxit khi nung chảy cao hơn khi sống trạng thái rắn bởi đó sẽ sở hữu được sắt oxit kết tinh vào men khi có tác dụng nguội, môi trường thiên nhiên oxy hoá hay khử. Men bao gồm hàm lượng hóa học chảy cao, tâm điểm chảy thấp đã hoà tan được nhiều sắt hơn.
Kẽm làm cho xấu màu sắc của sắt. Titan với rutil cùng với sắt rất có thể tạo công dụng đốm tuyệt vệt màu hết sức đẹp. Vào men khử (reduction glaze) có Fe2O3, men sẽ sở hữu màu từ bỏ ngọc lam mang đến xanh táo bị cắn (khi men bao gồm hàm lượng soda cao, có bo oxit). Trong men canxia, Fe2O3 có xu thế cho color vàng. Trong men kiềm cho màu từ đá quý rơm (straw yellow) mang đến vàng nâu (yellow brown). Men chì nung thấp, men kali với natri có red color khi thêm Fe2O3 (không bao gồm sự hiện hữu của bari).
Fe3O4 (oxit sắt từ) là tất cả hổn hợp của Fe2O3 với Fe
O, tác dụng của làm phản ứng biến đổi không hoàn toàn hay hoàn toàn có thể là dạng khoáng đồ dùng kết tinh từ nhiên, mang lại màu nâu. Dạng sau dùng để tạo đốm nâu lắt nhắt (specking) vào men.
Ngoài tính năng tạo màu, thêm Fe2O3 vào men giúp giảm rạn men (nếu hàm lượng áp dụng dưới 2%).
Sắt III Oxit màu gì? đặc điểm vật lý của fe III Oxit
Sắt 3 Oxit là hóa học rắn red color nâu, không tan trong nước.
Khối lượng mol 159,6922 g/molHệ số co và giãn nhiệt 12,5×10−6/℃Nhiệt độ nóng chảy 1565 ℃.
Tính chất hóa học của sắt bố Oxit
Sắt (III) có tính oxi hoá
– Khi tác dụng với chất khử, hợp hóa học sắt (III) bị khử thành hợp chất sắt (II) hoặc kim loại sắt từ do.
– vào pư hoá học, ion Fe3+ có chức năng nhận 1 hoặc 3e, tùy thuộc vào hóa học khử to gan lớn mật hay yếu:
Fe3+ + 1e → Fe2+
Fe3+ + 3e → Fe
=> tính chất chung của hợp chất sắt (III) là tính oxi hoá.
Sắt III oxit tính năng với dung dịch axit tạo ra dung dịch bazơ tạo nên dung dịch muối cùng nước
Fe2O3 + 6HCl → 2Fe
Cl3 + 3H2O
Fe2O3 + 3H2SO4 → 2Fe2(SO4) + 3H2O
Fe2O3 + 6HNO3→ 2Fe(NO3)3 + 3H2O
Ở nhiệt độ cao, Fe2O3 bị co hoặc H2 khử thành Fe
Fe2O3 + 3CO →to 3CO2 + 2Fe
Fe2O3 + 3H2 →to 3H2O + 2Fe
Fe2O3 bội phản ứng nhiệt độ nhôm
Fe2O3 + 2Al →to Al2O3 + 2Fe
Hợpchất sắt(III) gồm màu gì?
Tính hóa học hóa học đặc trưng của hợp chất sắt(III) là tính oxi hóa.
1. Sắt(III) oxit (Fe2O3)
Fe2O3 là hóa học rắn màu đỏ nâu, ko tan trong nước.
Fe2O3 là oxit bazơ yêu cầu dễ tan trong số dung dịch axit mạnh.
Ở nhiệt độ cao, Fe2O3 bị co hoặc H khử thành Fe.
Fe2O3 hoàn toàn có thể điều chế bởi phản ứng phân diệt Fe(OH)3 ở ánh nắng mặt trời cao.
Fe2O3 bao gồm trong tự nhiên dưới dạng quặng hematit dùng để luyện gang.
2. Sắt(III) hiđroxit (Fe(OH)3)
Fe(OH)3là chất rắn, gray clolor đỏ, ko tan trong nước dẫu vậy dễ chảy trong hỗn hợp axit tạo thành dung dịch muối sắt(III).
Sắt(III) hiđroxit được điều chế bằng cách cho dung dịch kiềm công dụng với dung dịch muối sắt(III).
Trong các công thức hóa học chúng ta phải nhận ra được công thức chất hóa học của sắt III oxit, để tò mò về Sắt III oxit là gì?
Màu gì? Mời những em cùng xem công thức, cấu tạo cũng như đặc điểm hóa học của hợp hóa học sắt III oxit tại trên đây nhé!
Sắt(III) oxit là gì?
Sắt(III) oxit (công thức Fe2O3) là một trong những oxit của sắt. Nó có trọng lượng mol 159,6922 g/mol, hệ số giãn nở nhiệt 12,5×10-6/℃, ánh nắng mặt trời nóng chảy 1565 ℃.
Về phương diện hóa học, fe oxit cũng thuộc đội oxit lưỡng tính như nhôm oxit. Fe2O3 ko phải là một trong những oxit dễ dàng chảy, nó là một oxit nặng nề chảy. Fe2O3 là dạng phổ biến nhất của sắt oxit trường đoản cú nhiên. Ngoài ra có thể lấy chất này từ đất sét nung màu đỏ.
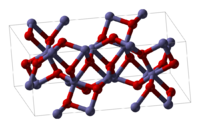 Cấu trúc tinh thể của hematit |
| Ferric oxit, Hematit, sắt oxit đỏ, synthetic maghemit, colcothar, sắt sesquioxit, ferrum(III) oxitferrum sesquioxit |
| 1309-37-1 |
| 518696 |
| NO7400000 |
| ảnh |
đầy đủ O1 |
đầy đủ 1/2Fe.3O/r Fe2O3/c3-1-4-2(3)5-1 |
| 21106565 |
| Fe2O3 |
| 159,6922 g/mol |
| chất rắn red color nâu |
| không mùi |
| 5,242 g/cm³, rắn |
| 1.566 °C (1.839 K; 2.851 °F) (phân hủy) |
| không tan |
| Ba nghiêng |
| -825,50 k J/mol |
| không phân loại |
| không cháy |
| Sắt(III) florua |
| Mangan(III) oxit Coban(III) oxit |
Trừ khi gồm ghi chú khác, dữ liệu được cung cấp cho những vật liệu trong tâm trạng tiêu chuẩn chỉnh của bọn chúng (ở 25 °C <77 °F>, 100 k Pa).   Tham khảo hộp thông tin |
Công thức chất hóa học của fe III oxit.
Sắt III oxit có 2 nguyên tố fe kết hơp cùng với 3 nhân tố O.
Hợp chất sắt (III) oxit là hợp chất trong số ấy sắt tất cả mức lão hóa +3.
Sắt 3 Oxit là 1 oxide của sắt.
Công thức hóa học: Fe2O3
Phân tử khối: 160 g/mol.
Trong vật liệu gốm
Các hợp chất sắt là những chất chế tạo màu phổ cập nhất trong ngành gốm. Sắt rất có thể biểu hiện khác biệt tùy thuộc môi trường thiên nhiên lò, nhiệt độ nung, thời hạn nung và tùy thuộc vào thành phần hoá học của men. Vày đó có thể nói nó là trong những nguyên liệu lý thú nhất.
Trong môi trường thiên nhiên nung khử, Fe2O3 thuận tiện bị khử (do cacbon hay các hợp chất lưu huỳnh trong nguyên liệu, trong môi trường xung quanh lò) thành Fe
O và phát triển thành chất chảy. Nếu còn muốn giữ được sắt(III) oxit, từ bỏ 700–900 ℃, môi trường xung quanh nung đề xuất là oxy hóa. Trong môi trường thiên nhiên nung oxy hóa, nó vẫn luôn là Fe2O3 và cho màu men tự hổ phách (amber) cho vàng nếu hàm lượng buổi tối đa trong men là 4% (rõ rệt hơn giả dụ men bao gồm chì oxit và can xi oxit), đến men màu domain authority rám nắng nóng (tan) nếu như hàm lượng khoảng tầm 6% và đến màu nâu nếu các chất Fe2O3 cao hơn.
Màu đỏ của sắt(III) oxit có thể chuyển đổi trên một khoảng rộng trong vòng nhiệt độ nung thấp bên dưới 1050 ℃. Nếu như nung rẻ thì có màu cam sáng. ánh nắng mặt trời tăng màu sắc sẽ chuyển sang đỏ sáng rồi đỏ sậm và cuối cùng là nâu. Chuyển đổi từ đỏ quý phái nâu xảy ra đột ngột trên một khoảng chừng nhiệt độ hẹp, cần lưu ý.
Hầu hết những loại men sẽ sở hữu được độ hoà tung sắt(III) oxit lúc nung chảy cao hơn nữa khi ngơi nghỉ trạng thái rắn vày đó sẽ sở hữu sắt oxit kết tinh trong men khi làm nguội, môi trường thiên nhiên oxy hoá hay khử. Men có hàm lượng chất chảy cao, điểm trung tâm chảy thấp đã hoà tan được không ít sắt hơn.
Kẽm có tác dụng xấu color của sắt. Titan và rutil với sắt rất có thể tạo kết quả đốm tuyệt vệt màu cực kỳ đẹp. Trong men khử (reduction glaze) tất cả Fe2O3, men sẽ sở hữu màu từ ngọc lam đến xanh táo (khi men gồm hàm lượng soda cao, gồm bo oxit). Vào men canxia, Fe2O3 có khuynh hướng cho màu sắc vàng. Vào men kiềm mang đến màu từ tiến thưởng rơm (straw yellow) đến vàng nâu (yellow brown). Men chì nung thấp, men kali với natri có màu đỏ khi thêm Fe2O3 (không gồm sự hiện diện của bari).
Fe3O4 (oxit fe từ) là các thành phần hỗn hợp của Fe2O3 với Fe
O, tác dụng của phản bội ứng đổi khác không hoàn toàn hay có thể là dạng khoáng thứ kết tinh từ nhiên, đến màu nâu. Dạng sau dùng để làm tạo đốm nâu lắt nhắt (specking) vào men.
Ngoài tính năng tạo màu, thêm Fe2O3 vào men giúp bớt rạn men (nếu hàm lượng sử dụng dưới 2%).
Sắt III Oxit color gì? tính chất vật lý của fe III Oxit
Sắt 3 Oxit là hóa học rắn màu đỏ nâu, ko tan vào nước.
Khối lượng mol 159,6922 g/molHệ số giãn nở nhiệt 12,5×10−6/℃Nhiệt nhiệt độ chảy 1565 ℃.
Tính chất hóa học của sắt cha Oxit
Sắt (III) có tính oxi hoá
– Khi công dụng với chất khử, hợp hóa học sắt (III) bị khử thành hợp chất sắt (II) hoặc kim loại sắt từ bỏ do.
– trong pư hoá học, ion Fe3+ có kỹ năng nhận 1 hoặc 3e, tùy thuộc vào hóa học khử táo bạo hay yếu:
Fe3+ + 1e → Fe2+
Fe3+ + 3e → Fe
=> đặc thù chung của hợp chất sắt (III) là tính oxi hoá.
Sắt III oxit tác dụng với dung dịch axit tạo ra dung dịch bazơ tạo ra dung dịch muối và nước
Fe2O3 + 6HCl → 2Fe
Cl3 + 3H2O
Fe2O3 + 3H2SO4 → 2Fe2(SO4) + 3H2O
Fe2O3 + 6HNO3→ 2Fe(NO3)3 + 3H2O
Ở nhiệt độ cao, Fe2O3 bị co hoặc H2 khử thành Fe
Fe2O3 + 3CO →to 3CO2 + 2Fe
Fe2O3 + 3H2 →to 3H2O + 2Fe
Fe2O3 bội phản ứng nhiệt nhôm
Fe2O3 + 2Al →to Al2O3 + 2Fe
Hợpchất sắt(III) gồm màu gì?
Tính hóa học hóa học đặc thù của hợp chất sắt(III) là tính oxi hóa.
1. Sắt(III) oxit (Fe2O3)
Fe2O3 là chất rắn màu đỏ nâu, không tan vào nước.
Fe2O3 là oxit bazơ buộc phải dễ tan trong các dung dịch axit mạnh.
Ở ánh nắng mặt trời cao, Fe2O3 bị teo hoặc H khử thành Fe.
Fe2O3 có thể điều chế bằng phản ứng phân hủy Fe(OH)3 ở ánh nắng mặt trời cao.
Fe2O3 có trong tự nhiên dưới dạng quặng hematit dùng làm luyện gang.
2. Sắt(III) hiđroxit (Fe(OH)3)
Fe(OH)3 là hóa học rắn, màu nâu đỏ, không tan vào nước nhưng lại dễ tung trong dung dịch axit tạo nên thành hỗn hợp muối sắt(III).
Xem thêm:
Sắt(III) hiđroxit được điều chế bằng cách cho dung dịch kiềm tính năng với dung dịch muối sắt(III).